Bando “Gruppi di Ricerca 2020” Progetto: A0375-2020-36583

Bando “Gruppi di Ricerca 2020”, Progetto: A0375-2020-36583
Titolo: Validazione di un nuovo anticorpo monoclonale multi-targeted per il trattamento di tumori e malattie retiniche – Acronimo: Politermab
Settore ERC: LS7_3 Pharmacology, pharmacogenomics, drug discovery and design, drug therapy.
Il progetto prevede la collaborazione tra:
- Dipartimento di Medicina dei Sistemi dell’Università di Roma “Tor Vergata”
- Istituto Dermopatico dell’Immacolata (IDI-IRCCS)
- Fondazione G.B. Bietti per lo Studio e la Ricerca in Oftalmologia-IRCCS
Il gruppo di lavoro è così composto:
- Prof.ssa Grazia Graziani (Professore Ordinario di Farmacologia, Dipartimento di Medicina dei Sistemi dell’Università di Roma “Tor Vergata”), responsabile scientifico del progetto
- Dott.ssa Rosella Cicconi (Univ. Roma Tor Vergata)
- Dott. Pedro Miguel Lacal (IDI-IRCCS)
- Dott.ssa Teresa Odorisio (IDI-IRCCS)
- Prof.ssa Monica Varano (IRCCS – Fondazione G.B. Bietti)
- Prof.ssa Mariacristina Parravano (IRCCS – Fondazione G.B. Bietti)
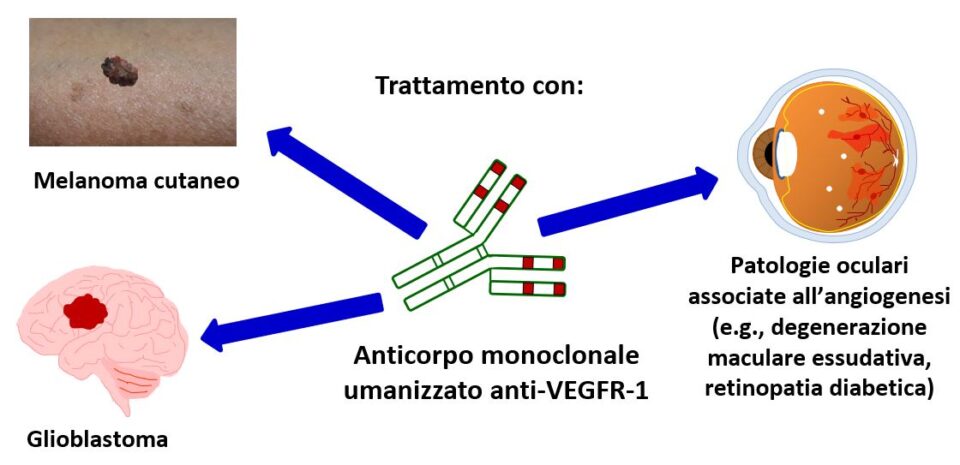
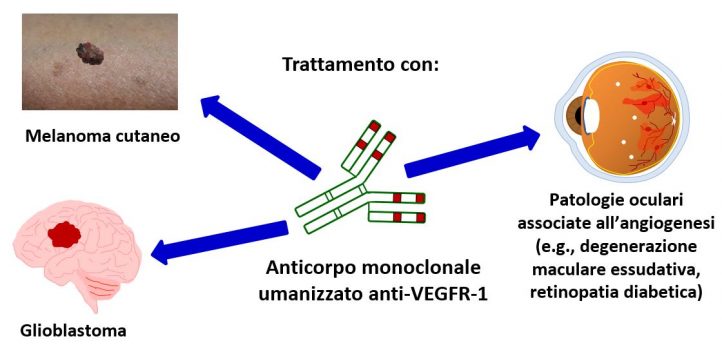
Il progetto di ricerca ha come obiettivo generale la valutazione della versione umanizzata di un anticorpo monoclonale (hD16F7), da noi generato, contro il recettore di tipo 1 del vascular endothelial growth factor (VEGFR-1), come agente terapeutico per neoplasie particolarmente aggressive (melanoma e glioblastoma) e retinopatie associate a vascolarizzazione aberrante.
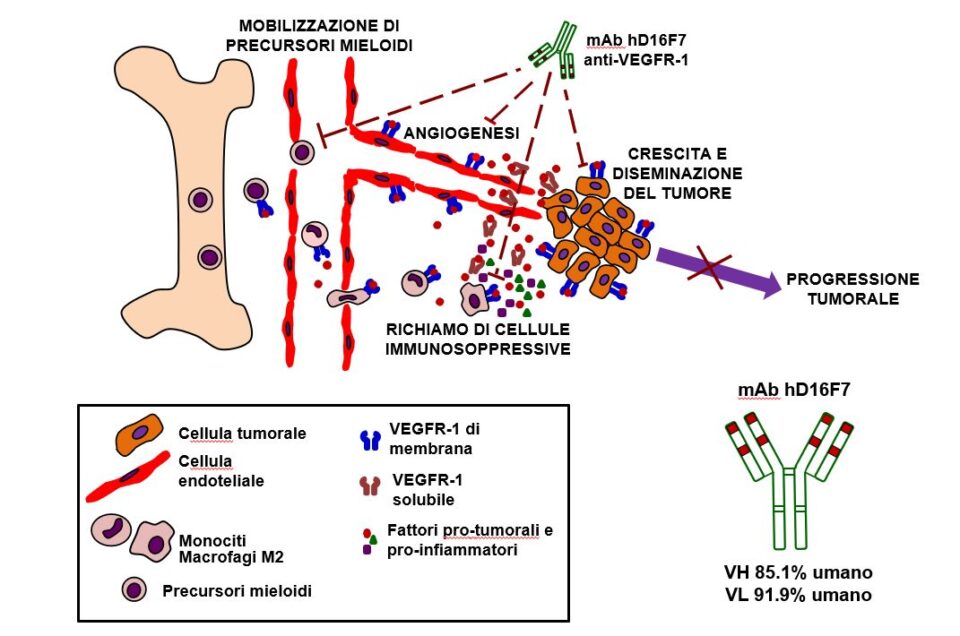
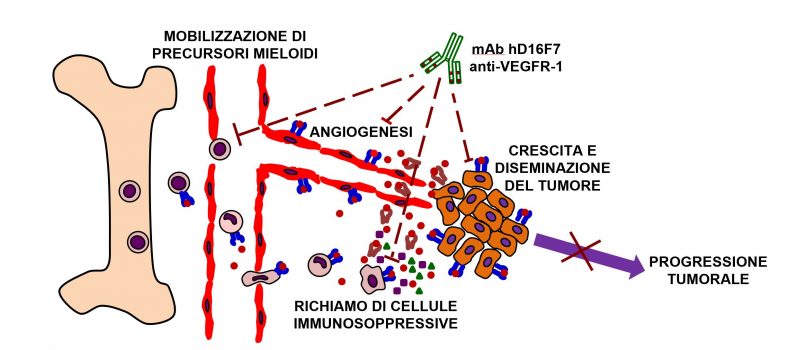
Il VEGFR-1 è un recettore tirosin chinasico di membrana stimolato da fattori di crescita angiogenici quali VEGF-A e il fattore di crescita placentare (PlGF). Il VEGF-A esercita la sua attività biologica anche attraverso un altro recettore di membrana, il VEGFR-2, mentre il PlGF lega esclusivamente il VEGFR-1, stimolando la permeabilità vasale, la neovascolarizzazione e l’infiammazione. Il VEGFR-1 svolge un ruolo rilevante nello stimolare l’angiogenesi patologica (e.g., associata alla crescita di tumori, retinopatie), mentre il VEGFR-2 regola sia l’angiogenesi fisiologica che quella patologica.
Oltre ad essere espresso nelle cellule endoteliali dei vasi sanguigni associati alla neoplasia, Il VEGFR-1 è espresso anche nelle stesse cellule tumorali (ad esempio melanoma e glioblastoma) e nei precursori midollari mieloidi ed a livelli elevati in monociti/macrofagi che infiltrano il tumore contribuendo alla progressione della malattia e resistenza a terapie mirate immunostimolanti o anti-angiogeniche.
Le strategie terapeutiche che bloccano il VEGF-A e conseguentemente la sua interazione con il VEGFR-2, quali quelle attualmente in uso, causano numerosi effetti indesiderati dovuti all’inibizione del ruolo fisiologico di VEGF-A. Al contrario, il blocco del VEGFR-1, non altera processi di angiogenesi fisiologica o altre funzioni del VEGF-A, quali ad esempio la regolazione della pressione arteriosa ed emostasi e la guarigione delle ferite.
Il VEGFR-1 svolge un ruolo importante anche nella progressione di retinopatie (sia di origine diabetica o relata all’età) associate alla neoformazione di vasi, che possono causare cecità irreversibile. È da sottolineare che nell’occhio il VEGFR-2 è espresso anche in cellule non vascolari, compresi i fotorecettori e le cellule gangliari in cui svolge una funzione neuroprotettiva, mentre il VEGFR-1 è localizzato prevalentemente nelle cellule endoteliali e nei periciti ed è implicato nel processo di angiogenesi patologica. Pertanto, da un punto di vista terapeutico a livello oculare la funzione del VEGFR-2 dovrebbe essere preservata, mentre quella del VEGFR-1 inibita. Invece, il blocco del VEGF-A, mediante somministrazione intravitreale di anticorpi monoclonali o frammenti anticorpali anti-VEGF-A, rappresenta l’attuale strategia terapeutica per ritardare la progressione della retinopatia associata ad angiogenesi aberrante.
È stato prodotto un anticorpo monoclonale umanizzato (hD16F7), a partire delle sequenze dell’anticorpo murino originale, per disporre di un prototipo che abbia le caratteristiche idonee per poter poi essere sottoposto a sperimentazione nell’uomo. Tale anticorpo, generato dall’Università di Roma “Tor Vergata” e l’IDI-IRCCS, e la produzione di frammenti da esso derivati, sono coperti da un brevetto nazionale (“Anticorpi anti-VEGFR-1 e usi di essi” N. 102016000034933) ed in fase di estensione alla zona europea (“Anti-VEGFR-1 antibodies and uses thereof”, n. PCT/IB2017/000379).
L’obiettivo del progetto consiste nella validazione in modelli preclinici in vivo dell’anticorpo anti-VEGFR-1 hD16F7 e di un suo derivato, come agenti terapeutici per neoplasie molto aggressive, quali melanoma e glioblastoma, e per retinopatie associate a neoformazione di vasi, comuni cause di cecità. In questo contesto, hD16F7 possiede un meccanismo di azione multi-targeted diverso da quello delle attuali terapie anti-angiogeniche oncologiche e di uso oculare poiché inibisce specificamente l’angiogenesi patologica e non quella fisiologica, l’invasività tumorale e l’infiltrazione del tumore da parte di cellule mieloidi ad attività immunosoppressiva.
La realizzazione del progetto comprenderà le seguenti fasi:
- Produzione in larga scala dell’anticorpo umanizzato hD16F7 per studi preclinici in vivo.
- Valutazione dell’efficacia di hD16F7 nel trattamento del melanoma, come agente singolo o in combinazione a BRAFi, sulla crescita del melanoma con mutazioni di BRAF, valutata utilizzando xenotrapianti di tumori ottenuti da pazienti.
- Valutazione dell’efficacia di hD16F7 nel trattamento del glioblastoma, da solo o in combinazione con temozolomide (chemioterapico di scelta nella terapia del glioblastoma), utilizzando modelli di linee cellulari umane di glioblastoma, resistenti o sensibili a temozolomide, impiantate in topi immunodepressi.
- Produzione e caratterizzazione di frammenti anticorpali variabili a singola catena (scFv) a partire da hD16F7, in quanto tali frammenti hanno una maggiore penetrazione attraverso gli strati retinici rispetto agli anticorpi monoclonali. Il frammento scFv prodotto sarà caratterizzato per capacità di legare VEGFR-1 (umano e murino) e di inibire l’angiogenesi.
- Validazione di frammenti scFv derivati da hD16F7 in un modello preclinico di retinopatia associata a neoformazione di vasi, mediante valutazione dell’efficacia del trattamento intravitreale con scFv sulla normalizzazione dei vasi retinici in topi transgenici che sovra-esprimono PlGF sotto il controllo del promotore della cheratina umana 14 (K14-PlGF).
I risultati attesi dallo sviluppo del progetto sottoposto sono:
- la validazione dell’anticorpo monoclonale umanizzato anti-VEGFR-1, hD16F7, in modelli preclinici in vivo di melanoma e glioblastoma umani;
- la produzione e validazione di frammenti variabili a singola catena scFv derivati da hD16F7, con maggiore penetrazione retinica, in un modello preclinico in vivo di retinopatia.
Questi risultati rappresenteranno la realizzazione di attività sperimentali volte alla dimostrazione di un “proof of concept” sperimentale.
Infine, grazie a questo finanziamento saranno attivati nei prossimi due anni 1 Assegno di Ricerca biennali (da parte dell’Università di Tor Vergata) ed 1 Contratto annuale di Ricerca (da parte dell’IRCCS Fondazione Bietti) per 2 ricercatori nel campo della ricerca relativa al progetto.
Il progetto, che ha una durata di 2 anni (data inizio: 15 Aprile 2021), ha ottenuto un finanziamento complessivo di 149.985,78 €
Collegamento alle pagine ufficiali dei fondi europei su www.europa.eu